回顾大健康――2021年12月医疗器械大事记
来源:中国经济网
中国经济网编辑:
今年12月《“十四五”医疗装备产业发展规划》发布,医疗器械领域首个国家产业发展规划为行业指明了方向;“一次手术破四个气球”引起热议,国家医保局组织调查;几个创新的医疗设备已经被批准.医疗器械多个领域的趋势反映了行业进一步发展的方向。中国经济网记者梳理了2021年12月医疗器械领域的重大事件,与读者一起回顾。
政策动态
《“十四五”医疗装备产业发展规划》已发布
12月28日,工信部、国家卫生健康委、国家发改委、科技部等10个部门联合发布《“十四五”医疗装备产业发展规划》。这是医疗器械领域的第一个国家产业发展规划。《规划》提出,到2025年,医疗器械产业先进,产业链现代化水平显著提升,主流医疗器械基本实现有效供给,高端医疗器械产品性能和质量水平显著提升,初步形成对公共卫生和医疗健康需求的综合保障能力。因此,《规划》部署了5项专项行动,分别是产业攻关、提升关键医疗设备供给能力、建设高端医疗设备应用示范基地、提升医学应急救援能力、完善医疗设备产业和应用标准体系。
国家医保局就“一个手术气球破四个气球”展开调查
12月28日,国家医保局有关部门负责人就有关媒体发布的《一台手术用破四个球囊!业内呼吁“低价中标”理念应客观评价》举报回答了记者提问。针对媒体报道“一次手术破了4个气球”,医保部门对媒体报道的相关情况进行了核实,并从所在医疗机构调阅了相关病历,了解了破裂气球产品的品牌、型号、批次。由首都医科大学国家医疗安全研究院组织,心血管领域10位专家对该病例进行背靠背的独立“双盲”评审,从手术中医疗器械的使用情况调查球囊破裂的原因;根据医疗器械质量抽查的有关规定,国家美国食品药品监督管理局委托上海美国食品药品监督管理局和广东美国食品药品监督管理局分别对相关产品进行质量抽查。从病历回顾来看,专家认为,由于患者血管弥漫性钙化严重,冠状动脉球囊扩张时容易被钙化部分刺破,球囊持续破裂与球囊质量无关,与病变及外科手术操作有关;专家排除了球囊破裂导致血管穿孔的可能,普遍认为血管损伤与术中操作有关。
扩大骨科耗材集中采购
12月23日,天津医药采购中心发布《关于开展骨科创伤类医用耗材关联十二省骨科创伤类医用耗材联盟带量采购中选目录工作的通知》。文件显示,此次由天津牵头的采购,与今年9月河南省牵头的骨科创伤耗材采购有关。通过招标,选择了71家企业的20751种产品,平均降幅为88.65%。其中,普通接骨板系统价格从4683元左右降至606元左右,平均降幅为87.05%;锁定(通用)加压钢板系统价格从约9360元降至约987元,平均降幅为89.45%。髓内钉系统价格从约11687元降至约1271元,平均降幅为89.12%。
工业趋势
浩海盛科收购南鹏光学。
12月1日,国内最大的眼科粘弹剂生产商、知名人工晶状体及视光材料生产商浩海柯胜发布公告称,其全资子公司浩海发展以总对价7000万元收购南鹏光学51%的股权,南鹏光学成为浩海发展的控股子公司。该交易的目的是
12月7日,国家医疗用品管理局宣布,经审查,批准北京米和医疗器械有限公司生产的创新产品“人工角膜”注册。适用于角膜移植难以成功的双眼角膜盲患者,包括角膜移植失败引起的严重角膜结膜瘢痕血管化、眼睑闭锁、严重自身免疫性疾病(如史蒂文斯-约翰逊综合征和瘢痕性类天疱疮)、化学伤、热烧伤和爆炸伤、终末期干眼症引起的角膜盲。该产品由人工材料制成,不需要供体角膜,有助于缓解我国角膜供体稀缺的现状。该产品为传统角膜移植禁忌症患者的临床治疗提供了新的途径。
创新产品“分支术中支架系统”获批。
12月16日,国家医疗用品管理局宣布,批准上海微创新麦医疗科技(集团)有限公司生产的创新产品“分支术中支架系统”注册.本产品适用于常规介入无法治疗的斯坦福A型和复杂斯坦福B型主动脉夹层的外科治疗。是国内首个获批上市的分支手术专用支架。其侧支结构可方便支架植入左锁骨下动脉,降低手术难度,减少左锁骨下动脉深度游离吻合带来的相关风险,惠及更多主动脉夹层患者。
华为医疗器械上市。
12月23日,华为在华为冬季旗舰新品发布会上正式推出手腕式心电血压记录仪——Huawei watch d(支持血压测量和心电采集)。该设备是今年华为通过食品药品监督管理局批准的二类医疗设备。根据国家美国食品药品监督管理局的信息,相关产品名称:腕式心电血压记录仪。适用范围:用于成人手腕心电数据的采集(不含自动分析诊断功能),适用于用示波法测量成人血压和脉率,其数值供临床参考。
产品质量和召回
国家美国食品药品监督管理局:39批次(台)产品不符合标准。
12月22日,国家美国食品药品监督管理局发布关于国家医疗器械监督抽检结果的通报(2021年第105号),其中指出,为加强医疗器械监督管理,保障医疗器械产品安全有效,国家医疗器械管理局组织对-谷氨酰转移酶检测试剂(盒)、半导体激光治疗机、鼻内窥镜等18个品种进行了产品质量监督抽检,共39批次。
西门子医疗解决方案美国公司自愿召回超声波诊断超声波系统。
西门子医疗系统有限公司反映,由于涉及特定型号和批次的产品,存在ACUSONSequoia系统软件版本使用2D手动描图功能测量时准确,但周长值有被高估的风险的问题。制造商美国西门子医疗系统有限公司主动召回DiagnosticUltrasoundSystem(注册号:国机集团20192060012)。召回等级为二级。
GEHealthcare主动召回了图像存档和通信系统。
通用电气医疗系统贸易发展(上海)有限公司报告称,由于涉及特定型号和批次产品的检验管理功能存在软件异常问题,制造商GEHealthcare主动召回影像存档与通讯系统(注册号:国机集团注20182701756)。召回等级为二级。
美敦力公司MedtronicMiniMed主动召回胰岛素注射泵InsulinPump。
美敦力(上海)管理有限公司报告称,MMT-503EU遥控器因涉及特定型号和特定批次产品,存在潜在安全漏洞。美敦力制造商美敦力MiniMed主动召回InsulinPump注射泵(注册号:国机集团20173141951)。召回级别为一级。
ArmstrongMedicalLtd有限公司主动召回二氧化碳吸收剂。
GE医疗系统贸易发展(上海)有限公司报告称,由于涉及特定型号和批次的产品,可能会导致意想不到的高气流阻力,这可能会影响或阻止麻醉患者充分通气的问题。制造商ArmstrongMedicalLtd主动召回二氧化碳吸收剂(备案证明代码:国机设备第20190776号)。召回级别为一级。
IntuitiveSurgical,Inc Intuitive Medical公司主动召回内窥镜手术器械控制系统的被动器械和附件。
直觉复星医疗器械科技(上海)有限公司报告称,由于无菌包装标签(托运箱和内箱标签)上的有效期错误问题,制造商直觉外科(IntuitiveSurgical,Inc .)直觉医疗公司主动召回内镜手术器械控制系统的无源器械及配件(注册号:国机注20172222398)。召回等级为二级。
BostonScientificCorporation主动召回导丝TransendGuidewire。
史赛克(北京)医疗器械有限公司举报称,BostonScientificCorporation生产的导丝批次因涉及特定型号和批次的产品,未经日本厚生劳动省批准,在灭菌场所进行灭菌。生产商BostonScientificCorporation主动召回导丝(注册号:国机注射20173770330)。召回等级为3级。
CooperVisionManufacturingLtd主动召回隐形眼镜护理液多用途解决方案。
固铂光学产品贸易(上海)有限公司报告称,由于误使用未经批准的高密度聚乙烯(HDPE)级材料制成的瓶子,CooperVisionManufacturingLtd主动召回隐形眼镜护理液多用途溶液(注册号:国机注20173221843)。召回等级为3级。
DePuy(爱尔兰)有限公司主动召回非无菌肩关节手术工具DePuy(爱尔兰)。
强生(上海)医疗器械有限公司报告称,由于涉及的具体型号和批次产品存在塞孔直径可能较小的问题,生产厂家DePuy(爱尔兰)有限公司主动召回肩关节非无菌手术工具DePuy(爱尔兰)(注册证号:国20191439)。召回等级为二级。
美敦力公司主动召回儿科充氧系统AFFINITYPIXIEOxygenationSystem。
美敦力(上海)管理有限公司报告称,美敦力公司的制造商美敦力公司(Medtronic Inc .)主动召回AFFINITYPIXIEOxygenationSystem(注册号:国机注20183102418),原因是该系统涉及特定型号和特定批次的产品。召回等级为3级。
(中国经济网记者韩伟综合整理)

-
鼓楼中国人寿携手光大银行华林分行推出“欢乐元宵·兔年元宵·祝福”客户联谊活动
2024-05-09
-
证监会对黄有龙赵薇孔德永分别采取5年证券市场禁入措施
2024-05-09
-
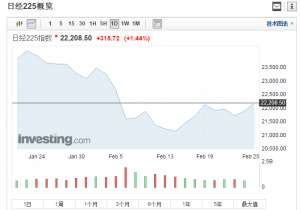
日韩股市周一双双高开 日经225指数涨幅扩大至1.44%
2024-05-09

-
量学扛鼎之作《股市天经:量波逮涨停》横空出世
2024-05-09

-
B站周三纳斯达克挂牌 一路下跌至2.26% 市值约31亿美元
2024-05-09
-
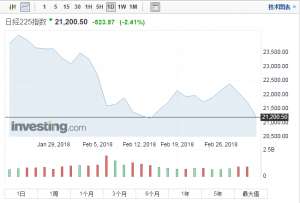
亚太股市继续走低,日本股市早盘大跌2% 东证股价指数开盘下跌1.65%
2024-05-09
